2023年8月末にホームページの「ペスト」の項目が急にみられるようになたので、何かと思い調べてみました。中国(モンゴル自治区内)とモンゴル(ウランバートル)で、新規のペスト罹患者が見つかったためでした。今のところ腺ペスト患者数名なので、封じ込めは可能ではないかと思われます。肺ペスト患者によるアウトブレイクでなければ、大丈夫と思いますが、注意は必要です。
ペストに関する原稿を依頼されました。以前、米国からのプレーリードッグの輸入を禁止する際に「プレーリードッグとペスト」の関連性を紹介しました。以下のインターネットにアップされています。http://hdkkk.umin.jp/topics/pest01.html
その後、千葉科学大学での「病原体の科学」で細菌の多様性、抗生物質と耐性菌、北里大学と千葉科学大学での「人獣共通感染症」で吸血昆虫(ベクター)の特徴、宿主齧歯類の多様性等を講義する間に、病原体の自然宿主、増幅動物、ベクター及びヒトでの振る舞いを少しづつ理解するようになりました。そうした観点で、複眼的に、この感染症「ペスト」を考えてみました。
ペスト
病原体
ペストの原因菌はグラム陰性、通性嫌気性の桿菌で、多くの病原菌が属するプロテオバクテリア門、腸内細菌科の細菌であり、特別な細菌ではない。分類学的にはプロテオバクテリア門、γプロテオバクテリア綱、エンテロバクター目、腸内細菌科、エルシニア属、エルシニア・ペスティス(Yersinia pestis)である。祖先といわれ、水系感染を起こす仮性結核菌(Yersinia pseudotuberculosis)に極めて近縁である。実際、両菌のゲノムはほとんど変わらないが、ペスト菌は仮性結核菌にはない2つのプラスミドを持っている。pPCP1(プラスミノーゲンアクチベータ、コアグラーゼ、ペスチシン1)、とpMT1(莢膜抗原、murin toxin)であり、これによりペスト菌が血液中で効率よく増殖するようになった。そのため砂漠周辺の草地あるいは山岳・森林地帯に生息する齧歯類を宿主としノミをベクターとして新たな生態系を確立したと考えられている。


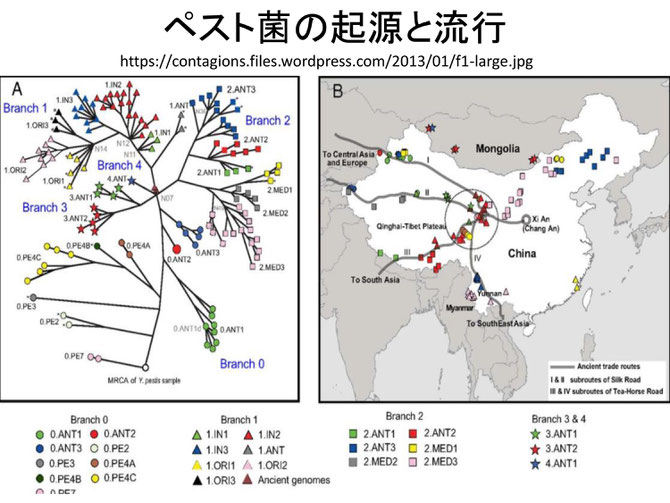
ペスト菌には3種類の病原性が異なる型がある。「ユスティニアヌス疫病」と言われ6~7世紀にシルクロードを介してヨーロッパに広がった古典型(Antiqua)、14世紀に「黒死病」として恐れられ、中世の大流行を引き起こした地中海型(Medievalis),および、19世紀以降の世界貿易の拡大に伴いネズミと共に世界中に拡散し、北里柴三郎とAlexandre Yersinによりペスト菌が分離された東洋型(Orientalis)である。
現在も世界各地で見られる流行は、このときの型(Orientalis)であり、アフリカの山岳地帯や密林地帯、東南アジアのヒマラヤ山脈周辺と熱帯森林地帯、中国、モンゴルの亜熱帯草原地域、中近東からカスピ海西北部、北米南西部ロッキー山脈周辺、南米北西部のアンデス山脈周辺と密林地帯で流行がみられる。病原性は一番古い流行型が最も強く、最後の流行型が最も弱い。いずれの型も中国の中西部に現存していると考えられている。

自然宿主とベクター
ペスト菌は自然界では齧歯類とノミの間で維持されている。一般にノミは、蚊やダニのような他の吸血ベクターと異なり、宿主域が狭い。例えば、ネコひっかき病のベクターとして知られているネコノミは、ヒトの血を吸うが、卵を産むにはネコへの吸血が必要であり、ヒトに持続的につくわけではない。また、ペスト菌を媒介するネズミノミも同様に、産卵のためにネズミから吸血する習性を持つと考えられている。
こうした特徴のためか、ノミは蚊やダニと異なり、細菌感染症であるエルシニア属による「ペスト」とバルトネラ属による「ネコひっかき病」、寄生虫症(条虫感染症)の「ウリザネ条虫症」以外、人獣共通感染症としてノミ媒介のウイルス病や原虫感染症は、ほとんど知られていない。
他方、自然宿主である齧歯類では、感受性の違いが知られている。北米ではプレーリードッグの他にジリス、リチャードソンジリス、ベルディングジリス、タウンゼンドジリス、ユインタジリス、カリフォルニアジリス、キンイロジリス、シマリス、ウッドラット、リスがペストの宿主となっている。ハタネズミやシカネズミのようなキャリアーの動物種(enzootic host)は、ペスト菌に対して比較的抵抗性が高く、繁殖力が高いので、ノミが通年をとおして活動し、ペスト菌を次世代の動物に移していくと考えられている。一方、非常に感受性が高く、致命的でペスト菌による敗血症を起こしやすい宿主(epizootic host)は、前述したジリス、リス、ウッドラット、プレーリードッグなどである。
ペスト菌の自然界での生態を考えると、ハタネズミやシカネズミがレゼルボアの役割を果たし、ペスト菌を維持している。高感受性のジリス、リス、プレーリードッグなどの増幅動物群に流行が広がると、ペスト菌の増殖が盛んとなり、直接あるいは伴侶動物やノミなどを介してヒトに感染が広がり、ヒト―ヒト感染に拡大すると考えられる。ペストは、しばしば南北アメリカ大陸、中国・インド・東南アジア、アフリカ大陸・マダガスカルなどで流行を起こしている。温暖化により大陸地域で乾燥地帯が拡大すると、齧歯類の生息域も変化を受け、ペスト菌を保有する動物とヒトとの接触機会が増加するリスクが考えられる。

流行疫学
ペストは、古くギリシアとスパルタが戦ったペロポネソス戦争の際のアテネでの流行(「アテネペスト」、科学的根拠はないが、そのように推察されている。天然痘、発疹チフスという説もある。)、東ローマ帝国ユスティニアヌス王朝の第2代皇帝(ユスティニアヌス1世)における腺ペストの流行が記載されている。後者は「ユスティニアヌス疫病」として知られ、ローマ帝国拡大・再統合の夢を断念する引き金となった。
14世紀の「黒死病」は、ベネチアの検疫制度の開始やイスラム圏の医学者イブン・アルハティーブの「ペスト流行時、衣類・食器・イヤリングへの接触が発症の有無を左右する」、イブン・ハーティマの「感染症は微生物が体内に侵入することによって発症する」といった、先進的なペストに関する流行疫学の発見を生んだ。しかし、この流行はアジア(中国)からシルクロードを経由して欧州(イタリア)に伝播し、当時の欧州の人口の3分の1から3分の2に当たる、約2,000万から3,000万人が死亡したと推定されている。また全世界では、約8,500万人~1億人が死亡したと考えられる大流行であった。
3回目の大流行は現在に続くものである。中国雲南省で1855年に大流行した腺ペストを起源とするものであり、香港での大流行(1894年)をきっかけとして拡大し、台湾、日本、ハワイ諸島、米国、東南アジア、南アジアの各地に広がった。1910年からは清朝末期の満州で肺ペストが流行した。またインドでの死亡者は1200万人以上に達したといわれている。
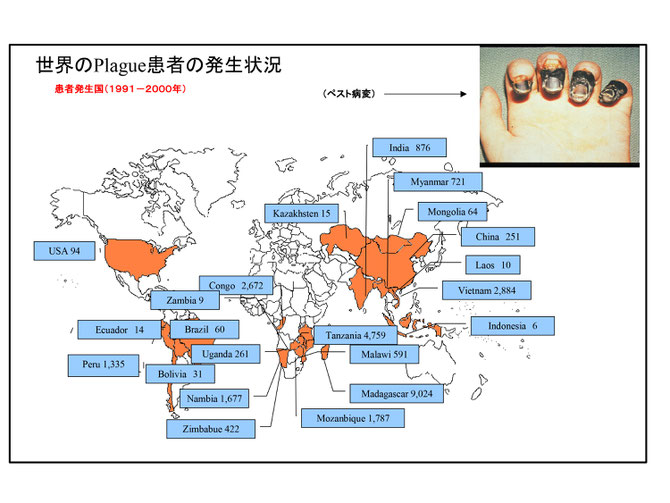
前述したように、ペストは決して過去の疾病ではない。現在でも世界の多くの国々で発生している。1991年から2000年の間に、アフリカ大陸ではマダガスカルの9,000人、タンザニアの4,700人をはじめ、モザンビーク、コンゴ、ナムビアなどで1,000人以上の患者が出ている。アジア大陸ではベトナムの2,900人、インドの900人の他に、ミヤンマー、モンゴル、中国、カザフスタン、インドネシアなどで発生が見られている。アメリカ大陸では米国が100人、南米ではペルーの1,300人、ブラジルの60人の他、エクアドル、ボリビアで流行が見られた。
感染症統御が最も進んでいると考えられる米国では、1970年から1994年の間に、ヒトペストの原因動物として同定されたケースは、リスが44.3%、プレーリードッグが5.7%、ウサギ6.9%、ネコ5.3%、その他の肉食動物2.7%と報告されている。通常、enzootic hostからヒトが感染することはなく、ヒトへの感染はepizootic hostから直接、あるいは伴侶動物などの他の動物種をとおして感染する。また、1959年から1998年まで米国では393例のペスト患者の発生が報告されており、そのうち240例で感染源が同定されている。プレーリードッグあるいはそのノミから、ヒトに感染した例は31例であった。また、米国でのペスト発生州は経年的に増加しており、1995年~97年に発生したヒトの18症例のうち5例はプレーリードッグを介したものであり、2例は死亡している。1998年5月にはテキサス州でノミを駆除し、10日間の検疫後に売買された356頭のプレーリードッグのうち223頭が輸送後に、ペストを発症するというケースが報告されている。
2000年以降も世界的にペストの散発がみられている。特にマダガスカル、コンゴ、ペルー、米国では毎年発生が報告されている。2010年~2015年には世界で3,248人の患者が報告され、548人が死亡した。直近では、マダガスカル山岳部で恒常的に腺ペストの発生が見られていたが、2017年8月以降に首都アンタナナリボを含めた都市部での肺ペスト患者の増加が見られており、10月8日までに肺ペスト患者 227人、腺ペスト患者106人、ペスト敗血症1人の発生が確認され、45人が死亡した。世界保健機関(WHO)がマダガスカルのペストと戦うために、120万ドーズに近い抗生物質を提供し、150万ドルの緊急資金を提供した。WHOは、マダガスカルのペストのアウトブレイクに効果的に対応し、命を救うために550万ドルの資金が必要であることをアピールしている。
一般的に、ペスト菌のヒトへの感染経路としては、病原体保有ノミ刺咬による感染が78 %、ペットなどを含む感染小動物の体液を介した傷口からの感染が20 %、ペスト菌含有エアロゾルの吸入が2 %(肺ペストによるヒトからヒトへの感染)となっている。また、流行の常在地域でのペスト患者の発生はノミの活動期(高温・多湿、6~8月)に集中する傾向がみられる。

症状
ペストの臨床症状には、腺ペスト、敗血症ペスト、肺ペストの3種類が知られている。
腺ペストの潜伏期間は2日~7日であり、ペストの80 ~90 %を占める。感染齧歯類などに吸着したノミによる刺咬後に発病する最も一般的な型である。稀に、感染したヒトあるいは動物への接触により、傷口や粘膜から感染する場合もある。急激な発熱(38 C 以上の高熱)、頭痛、悪寒、倦怠感、不快感、食欲不振、嘔吐、筋肉痛、疲労衰弱などの強い全身症状、さらに鼠径部、腋窩、頸部などの局所リンパ節腫脹(クルミ~アヒルの卵大)および壊死・膿瘍形成が特徴である。発症後、ペスト菌はリンパ流、血流を介して脾臓、肝臓、骨髄、心臓、肺臓など全身に伝播して敗血症を起こす。第3~4 病日に敗血症を起こし、その後2~3日以内に死亡する。ノミの刺咬部位には変化はないが、稀に、刺咬部位の皮膚、または眼に化膿性潰瘍や出血性炎症を形成する場合があり、皮膚ペスト、眼ペストと呼ばれている。
敗血症ペストはペストの約10 %を占める。局所症状がないまま全身にペスト菌が伝播して敗血症を引き起こす場合、腺ペストから敗血症への移行によるものがある。急激なショックおよびDIC(播種性血管内凝固)、昏睡、手足の壊死、紫斑など、いわゆる「黒死病」を起こす。通例、発症後2~3日以内に死亡する。
肺ペストは、腺ペストの末期や敗血症ペストの経過中に起こる。増殖したペスト菌が肺に侵入して肺炎を起こし、肺胞が壊れて、痰やペスト菌含有エアロゾルを排出するようになる。この場合、肺ペスト患者が感染源になって、ペスト菌がヒトからヒトへ素早く伝播する。肺ペスト患者のペスト菌含有エアロゾルを吸い込んで2 次的に発症すると、強烈な頭痛、嘔吐、39 ~41 C の高熱、急激な呼吸困難、鮮紅色の泡立った血痰を伴う重篤な肺炎が起こる。潜伏期間は通例2~3日、最短は12~15時間。発病後12~24時間で死亡する。

診断
診断には、血液や腫脹したリンパ節の吸引物、痰などにペスト菌を証明する。患者血清中の抗Fraction 1 抗体価が、受身赤血球凝集(PHA)反応で10 倍以上上昇する。PCR によりペスト菌の遺伝子を確認する等の方法がある。
行政的な、疑似患者と確定患者の診断基準は以下のように定められている。
1、疑似患者:ペスト流行地への渡航歴や、バイオテロに巻き込まれた可能性がある場合で、ペストの臨床症状を示し、臨床材料からグラム陰性で両端染色性を示す桿菌や、診断用抗原(莢膜抗原)に対する抗体、蛍光抗体に対して陽性を示す菌が検出された場合。あるいは、ペスト菌に特異的なプライマーを用いたPCR 法で、特異的なバンドが検出された場合、患者血清中の抗Fraction 1 抗体価が、PHA反応で16 倍以上を示した場合。
2、確定患者:臨床材料から分離した菌が、顕微鏡所見で明らかな極小体を示すグラム陰性桿菌で、莢膜抗原に対する抗体、蛍光抗体に陽性を示し、ペスト菌に特異的なプライマーを用いたPCR 法で陽性を示し、ペスト菌特異ファージに対して感受性を示し、生化学的性状がペスト菌の性状と一致することなどから総合的に判断し、ペスト菌(Yersinia pestis)と同定された場合。あるいはPHA反応で、診断用抗原に対する回復期の抗体価が、感染初期の抗体価の4 倍以上上昇している場合。

治療
幸いペスト菌は多くの抗生物質に感受性であるが、治療が遅れると非常に高い致死率を示す。回復後、予後は良好で、後遺症は殆ど残らない。日本でペストの治療薬として保険が適用されるのは、ストレプトマイシンだけである。ペストに最も効果があるが、副作用があるので過度の投与は避けたほうが良い。新生児、未熟児、乳児、小児に対する安全性はまだ確立されていない。
他方、米国疾病予防管理センター(CDC)、WHO が推奨する抗生物質には以下のものがある(治療期間はすべての抗菌薬において10 日を超えないこと)。また、テトラサイクリンに対する耐性を持つペスト菌の報告があるので注意が必要である。
1、アミノグリコシド系(蛋白合成阻害):ストレプトマイシン、ゲンタマイシンは全てのペストに最も効果がある。
2、テトラサイクリン系(蛋白質合成阻害):テトラサイクリン、ドキシサイクリンは腺ペストおよび肺ペストの治療にアミノグリコシド系と適宜併用。
3、クロラムフェニコール(蛋白質合成阻害):ペストの髄膜炎、胸膜炎、内眼球炎等の治療に用いる。腺ペスト、敗血症型ペストには、アミノグリコシド系と適宜併用。
4、ニューキノロン系(DNA合成阻害):全般的にペストに対して優れた効力を示す。特にレボフロキサシン、スパルフロキサシンが優れている。副作用の強いアミノグリコシド系よりペストの治療に期待が持てる。
予防
患者と直接接触した人や肺ペスト患者に接近した人など、発病する可能性の高い人や、流行地への旅行者などのように短期間ペストの暴露を受ける可能性がある人に対して、予防のためにWHO、CDC は抗菌薬(テトラサイクリン、ドキシサイクリン、ST合剤(サルファメソキサゾールとトリメトプリムを5対1の比率で配合した合剤))の予防投与を勧めている。投与量は、治療で用いる量の1/2 ~同量を経口投与する。
米国からのプレーリードッグの輸入を禁止する際に「プレーリードッグとペスト」の関連性を紹介しました。以下のインターネットにアップされています。やってみると、うまくつながらないケースがあるので、ここにもう一度アップしておきます。調べてみると2003年の原稿でした。
ペストとプレーリードッグ
東京大学大学院農学生命科学研究科 吉川泰弘
はじめに:1999年の感染症新法制定の際、動物由来感染症が始めてヒトの感染症法の対象になった。最も厳しい対応を必要とする第1類感染症としてエボラ出血熱、マールブルグ病、クリミア・コンゴ出血熱、ラッサ熱のようなウイルス性出血熱と細菌感染症であるペストが対象となった。これらはいずれも動物由来感染症であるが、このときの政令では、サル類のエボラ出血熱とマールブルグ病が指定動物および指定感染症として定められ、原則輸入禁止あるいは法定検疫の対象とされた。
ペストに関しては1999年11月CDCがわが国に輸入されるプレーリードッグにペスト感染のリスクがあることを伝え、国立感染症研究所と厚生省(現厚生労働省)に検討会・調整会が置かれた。1999年と2001年に厚生科学研究費で輸入プレーリードッグのリスク評価が行われ、輸入規制の必要性が提言された。他方、2001年から財務省がげっ歯類の輸入統計を開始し、2002年4月に年間1万3千頭以上が輸入されていることが明らかになった。2002年7月輸入動物に関する規制検討委員会が発足し、また厚生科学審議会感染症分科会感染症部会に動物由来感染症ワーキング・グループ(WG)が設置された。このWGは、1999年に施行された感染症法の5年後見直しのための検討を進める目的で組織されたものである。2002年8月米国のプレーリードッグ輸出施設で野兎病が発生し、CDCは国立感染症研究所に連絡してきた。厚生労働省は国内の輸入業者に連絡し自治体の協力を得て調査し、異常がないことを確認したが、個人に販売されたプレーリードッグの行方を把握することは困難であった。

野兎病はダニ等により媒介される細菌性の動物由来感染症である。ペストはノミによって媒介されるが、輸出施設で野兎病が発生したことは、同じ節足動物で媒介されるペストのコントロールが出来ていないことを意味する。WGはリスクの大きさを考え、感染症部会を介して厚生労働省にプレーリードッグのペストを政令で指定動物と指定感染症の対象にし、輸入禁止措置をとるべきであることを提言した。この提案は2003年1月末の閣議で了承され、2003年3月1日からプレーリードッグの輸入禁止措置が取られることとなった。
ペストとは?古くて新しい感染症:ペストは中世に黒死病と恐れられたあのペストである。ペストの歴史を振り返ると、その大流行は世界史上3回知られている。流行はいずれも中国を起源にしていると考えられる。6~7世紀シルクロードを介してヨーロッパに広がった古典型(Antiqua)、14世紀の中世の大流行を起こした地中海型(Medievalis),および、19世紀以降の世界貿易の進歩に伴いネズミと共に世界中に拡散した東洋型(Orientalis)である。現在の世界各地で見られる流行株はこのときの株である。病原性は一番古い流行株が最も強く、最後の流行株が最も弱い。いずれの株も中国の中西部に現存していると考えられる。
ペストの原因菌はエルシニア・ペスティ(Yersinia pesti)で、先祖は肉眼病変の類似性から偽結核(仮性結核とも言われる)の原因菌であるYersinia pseudotuberculosis と考えられている。反芻動物の結核に類似したヨーネ病は、パラ結核といわれるミコバクテリウム・パラツベルクローシス(Mycobacterium paratuberculosis)により引き起こされる。名前も病変も似ているので、しばしば混同される。偽結核菌は水系感染(水路を介した伝播)を起こすが、ペスト菌は血液中でよく増殖できるように新たなプラスミドを獲得した。そのため砂漠近郊に生息するげっ歯類を宿主としノミを媒介動物として新たな生態系を確立したと考えられている。
ペストは決して過去の疾病ではない。現在でも世界の多くの国々で発生している。1991年から2000年の間に、アフリカ大陸ではマダガスカルの9000人、タンザニアの4700人をはじめ、モザンビーク、コンゴ、ナムビアなどで1000人以上の患者が出ている。アジア大陸ではベトナムの2900人、インドの900人の他に、ミヤンマー、モンゴル、中国、カザフスタン、インドネシアなどで発生が見られている。アメリカ大陸では米国が100人、南米ではペルーの1300人、ブラジルの60人の他、エクアドル、ボリビアで流行が見られた。決して過去の疾病ではない。幸いペスト菌は多くの抗生物質(ストレプトマイシン、テトラサイクリン、クロラムフェニコールおよびニューキノロン系)に感受性であるが、治療が遅れると非常に高い致死率を示す。また肺ペストの場合はエロゾールで感染が拡がるので注意が必要である。
ペストとプレーリードッグ:プレーリードッグはげっ歯類、リス科の動物である。北米中西部(アリゾナ、コロラド、ユタ、オクラホマなど)を中心に米国からカナダに広く分布し、オグロプレーリードッグ、オジロプレーリードッグ、ガニソンプレーリードッグ、ユタプレーリードッグ、メキシコプレーリードッグが生息している。わが国には主としてオグロプレーリードッグとオジロプレーリードッグがペットとして輸入されている。
ペストは前述したようにげっ歯類とノミの間で維持されている。北米ではプレーリードッグの他にジリス、リチャードソンジリス、ベルディングジリス、タウンゼンドジリス、ユインタジリス、カリフォルニアジリス、キンイロジリス、シマリス、ウッドラット、リスがペストの宿主となっている。キャリアーの動物種(enzootic host)はペスト菌に対して比較的抵抗性が高く、繁殖力が高いので、ノミが通年をとおして活動し、ペスト菌を次世代の動物に移していくと考えられる。ハタネズミやシカネズミがこれにあたる。他方非常に感受性が高く、致命的でペスト菌の敗血症を起こしやすい動物種(epizootic host)は、前述したジリス、リス、ウッドラット、プレーリードッグなどである。
米国では1970年から1994年の間に、ヒトペストの原因動物として同定されたケースはリスが44.3%、プレーリードッグが5.7%、ウサギ6.9%、ネコ5.3%、その他の肉食動物2.7%などである。通常、enzootic hostからヒトが感染することはなく、ヒトへの感染はepizootic hostから直接、あるいは伴侶動物などの他の動物種をとおして感染する。1959年から1998年まで米国では393例のペスト患者の発生が報告されており、そのうち240例で感染源が同定されている。プレーリードッグあるいはそのノミから、ヒトに感染した例は31であった。また図のように、米国でのペスト発生州は経年的に増加しており、1995年~97年に発生したヒトの18症例のうち5例はプレーリードッグを介したものであり、2例は死亡している。1998年5月にはテキサス州でノミを駆除し、10日間の検疫後売買された356頭のプレーリードッグのうち223頭が輸送後ペストを発症するというケースが報告されている。

プレーリードッグのペスト:春から夏にかけて、ノミの活動が活発なりに、その年の初子が自由に動き回る時期(3月~5月)に流行が起こることが多い。潜伏期間は明瞭ではないが、プレーリードッグは感受性が高く1週間から2週間以内と考えられる。発症した場合はほぼ100%死亡する。特にペスト特有の臨床症状は知られていない。野生げっ歯類では行動異常が認められるという報告がある。リンパ節の腫脹、鼻出血が認められる場合もある。しかし、一般には明らかな臨床症状は示さないで、突然死亡することが多い。
プレーリードッグはペストに対する感受性が非常に高いので、国内に輸入され、長期間飼育されている個体がペストに感染していたり、ペスト菌を保有していることはあり得ない。しかし、輸入直後に原因不明で死亡した場合にはペストも疑う必要がある。
診断:死亡個体に関しては直接ペスト菌の莢膜抗原(fraction 1)を蛍光抗体法(直接法)で検出する。死後時間が経過していても骨髄から材料採取すると検査に使える。確定診断はペスト菌の分離、PCR法による遺伝子検出である。検査は地方自治体の衛生研究所で可能。
病理:プレーリードッグのペスト病変に関する記載はほとんどない。しかし、感受性の高い他のげっ歯類と類似していると考えられる。カリフォルニアジリスの場合は急性感染では出血性リンパ節炎、脾腫などが見られる。亜急性例では壊死性リンパ節炎、肝・脾の結節性巣状壊死。治癒例では化膿性巣状壊死を伴うリンパ節腫脹が見られている。他に、肺炎、鼻出血、胸部点状出血、脾の膿瘍などが認められたケースがある。
おわりに:2003年3月1日からプレーリードッグは上述の理由から輸入禁止動物となった。従って、今後プレーリードッグに由来するペストの侵入が起こることは考えられない。しかし、プレーリードッグは既にエキゾチックペットとして、安定した人気を持っており、ニーズも高い。安全な個体を飼育するには繁殖個体を購入するか、検疫が始まれば検疫済みの個体を購入することになる。輸入検疫等に必要な条件に関しては現在検討中であるが、概ね以下のようなステップが必要とされると考えられる。
後期:その後、齧歯類は繁殖個体しか輸入できないことが法律で定められたために、北米からの捕獲プレーリードックの輸入はなくなった。欧州(オランダなど)で繁殖されたプレーリードックが輸入されるようになった。

参考文献:渡邊治雄 ペスト 感染症の診断・治療ガイドラインpp56-59日本医師会
山田章雄、渡邊治雄 プレーリードッグのペスト 同上 日本医師会
ペストについては、別の原稿(2015年)もありました。ここにアップしておきます。
歴史を変えた細菌 ~ペスト菌
ペストは、ペスト菌という細菌の感染によって起こる致命的な感染症です。ペストは齧歯類から蚤を介して感染します。ツキジデスによるペロポネソス戦争の記録にアテネでのペストの流行と思われる記述があります。また、中世の市民を恐怖のどん底に陥れた「黒死病」としても有名です。中世のペストの悲惨な様子は、ボッカチオの「デカメロン(十日物語)」やカミュの「ペスト」に書かれています。

ペストの流行の歴史を振り返ると、大流行は世界史上3回知られています。6世紀ユスティニアヌス帝の時に中近東、欧州、アジアに広がった古典型、14世紀の中世の大流行を起こした地中海型と、19世紀以降の世界貿易の拡大に伴いネズミと共に世界中に蔓延した東洋型です。しかし、現在でもアフリカ、アジア、アメリカ大陸には汚染地帯が存在し、野生の齧歯類と蚤の間でペスト菌が循環しています。1980年~1994 年の15 年間に世界保健機関(WHO)に報告されたペスト患者は、24 カ国で18,739 人、死亡者は1,852 人です。世界では、毎年のように地域的な流行を起こしています。決して歴史に埋もれた過去の感染症ではありません。

例えばインターネットでみれば以下のような記事が見られます。「マダガスカル保健省は、同国におけるペストの流行により、2013年9月以降319名が感染、75名が死亡していることを公表しました。またWHOの統計によれば、2012年のマダガスカルのペスト感染者は256名で、60名が死亡しています」。「米国では2006年ヒトのペスト症例が4州から計13例報告されています。ニューメキシコ州7例、コロラド州3例、カリフォルニア州2例と、テキサス州1例で、このうち死亡例は2例です」。

ペスト菌の生態と感染経路
ペスト菌は腸内細菌科に属します。グラム染色陰性の好気性の短桿菌です。細菌は基本的に3つの要素で分類します。形(丸い球菌、棒状の桿菌、螺旋状の螺旋菌など)と、呼吸系(酸素を必要とする酸素呼吸:好気性か、酸素を嫌う嫌気性呼吸か)とグラム染色です。グラム染色は、デンマークの医師ハンス・グラムが考案した細菌の最も基本的な染色方法です。細菌の細胞壁がクリスタルバイオレットという紫色の染色液で染まることを利用しています。ペニシリンは細菌の細胞壁の合成を阻害する抗生物質です。紫色に染まる細菌はグラム陽性で、ペニシリン等に感受性を示します。このような利点があるので、1884年に開発されて以来、現在でも使われています。
ペスト菌の学名はエルシニア・ペスティスで、その祖先は仮性結核菌(偽結核菌)と考えられています。ペスト菌と仮性結核菌の違いは、毒性をもつ1つのプラスミドがあるかないかの違いだけです。プラスミドは細菌や酵母などの染色体DNAとは別にあるDNAで、染色体とは独立して複製し、細胞分裂に伴って次の細胞に継がれていくDNA分子です。プラスミドのうえには抗生物質の耐性遺伝子や毒素遺伝子が載っていて、これらの形質を細菌から細菌に伝播する特性を持っています。つまり、ある細菌が獲得した形質を、別の細菌に伝えることが出来るのです。仮性結核菌は野生の齧歯類や食肉類の動物などが保有していて、冬場には飲み水を介して広がります。霊長類は感受性が高く、動物園などでは飼育しているサル類が集団感染を起こし、問題となる例が報告されています。また、ヒトでは食中毒を起こすエルシニア腸炎菌が同じグループに属します。
仮性結核菌は、水系感染(水を介した伝播)を起こしますが、ペスト菌はヒトを含め動物の血液中で非常によく増殖することができます。これは仮性結核菌が新しい病原プラスミドを獲得した結果、血液を介する感染ができるようになり、水の少ない砂漠近郊に生息する齧歯類を宿主とし、蚤を媒介動物として新しい生態系を確立したためと考えられています。
ペスト菌は感受性の低い野生の齧歯類と蚤の間で維持されており、感受性の高い野生の齧歯類(プレーリードッグなど)では、周期的な流行によるペスト菌の増幅が起こります。プレーリードックはペットとしても飼育されるので、ネコ、ウサギ等が巻き込まれることがあります。まれですが、感染ネコが肺ペスト様症状を示し、飛沫感染等で飼い主や獣医さんが感染した例があります。統計的には、蚤による感染が78 %、ペットなどからの感染が20 %、ペスト菌を含むエアロゾル(PM2.5のように空中を漂う微小粒子)の吸入による感染が2 %です。
ペストとは?
1999年、感染症法を制定した時、患者を指定病院に隔離するという最も厳しい対応が必要な1類感染症には、エボラ出血熱、マールブルグ病、クリミア・コンゴ出血熱、ラッサ熱のようなウイルス感染症が入りました。しかし、ただ一つ、細菌感染症であるペストが1類感染症に入っています。ウイルスは生きた細胞がなければ増殖できません。細胞内で増殖するので細胞を壊さないでウイルスを殺すことは困難です。そのため感染後の治療よりもワクチンのように感染予防に重点を置きます。細菌は栄養素があれば自分で増殖できます。また動物細胞にない細胞壁や独自の高分子合成機構を持っています。そのためヒトには無害で細菌を殺す抗生物質などがあります。ペストが1類感染症に入るのは、抗生物質による治療が間に合わないほど速く血液中で増えるためです。ヒトが感染し肺ペストになると呼吸器感染をおこすので、そのリスクは非常に高いものとなります。約20年前にインドで肺ペスト患者が出たときは、各国がインドからの飛行機の乗り入れを止めてしまいました。
世界でみればペストは、五つの地域において野生の齧歯類の間で小規模な流行を起こし、維持されています。南アフリカ地方およびマダガスカル、ヒマラヤ山脈周辺からインド北部、中国の雲南省からモンゴル、北米南西部ロッキー山脈地方および南米北西部アンデス山脈地方です。
ヒトがペスト菌に感染した後の潜伏期間は、1週間以内(2~7日)です。ペストは臨床症状によって、リンパ節を巻き込む腺ペスト(昔、リンパ節はリンパ腺といわれたためこの名前があります)、血液中でペスト菌が増殖する敗血症ペストと肺でペスト菌が増える肺ペストに分けられます。腺ペストはペストの80 ~90 %を占めます。38 ℃ 以上の急激な発熱、頭痛、悪寒、倦怠感、食欲不振、嘔吐、筋肉痛、疲労・衰弱などの強い全身症状、さらに鼠径部、腋窩、頸部などのリンパ節腫脹と膿瘍がみられます。敗血症ペストはペストの約10 %を占めます。腺ペストの後、ペスト菌が血流を介して全身に回り菌血症(敗血症)へと進行するものです。急激なショックと全身の小血管で血液が固まってしまう播種性血管内凝固(DIC)が起こります(播種性というのは、全身に広がることを意味します)。部分的に血流が止まってしまうので手足の壊死、紫斑などいわゆる「黒死病」の症状が起こり、昏睡状態に陥ります。肺ペストは、腺ペストの末期や敗血症ペストの経過中に起こります。ペスト菌が肺に侵入し、肺で増殖するものです。肺ペスト患者から排出されるペスト菌を含んだエアロゾルを吸い込むと二次感染が起こります。強烈な頭痛、嘔吐、39 ~41 ℃ の高熱、急激な呼吸困難、鮮紅色の泡立った血痰を伴う重篤な肺炎が起こります。
治療しないと腺ペストで90%が死亡、敗血症、肺ペストではほぼ100%死亡します。治療した場合の死亡率は5~20%といわれています。ペスト菌への暴露歴、臨床症状、血液・リンパ節吸引物・痰などからのペスト菌の分離により診断します。患者血清中の抗体価の上昇、ペスト菌の遺伝子増幅による遺伝子検出も有効です。治療法としてはクロラムフェニコールなど多くの抗生物質が有効です。しかし、ペニシリン系は無効なので注意が必要です。幸いわが国では1926 年以来、ペスト患者の報告はありません。予防にはワクチンがありますが日本では使用されていません。
ペスト流行の歴史
紀元前431年~404年、古代ギリシアで、2大勢力が激突したペロポネソス戦争がありました。これは、アテネを中心としたデロス同盟とスパルタを中心としたペロポネソス同盟の間に起きたものです。全古代ギリシアを巻き込んだ大戦争となりました。しかし、開戦の翌年(紀元前430年)に、アテネは感染症の大流行という不運に見舞われました。これが、ペストと考えられています。
ペストはアテネの外港ピレウスで始まり、アテネに伝播しました。不衛生な籠城生活を強いられていたアテネでは、感染症が非常な勢いで広まり、2年間で全人口の3分の1が死んだといわれています。ペストの流行は紀元前430~前426年まで続き、アテネは疲弊しました。紀元前405年、最後の海戦に敗れたアテネは海上から封鎖され、食料も尽き、紀元前404 年に降伏しました。こうして、ペロポネソス戦争はスパルタの勝利で終わりました。
古代アテネの歴史家ツキジデス(紀元前460~395年)は、この戦史の中で、アテネの疫病についてと「疫病から回復したヒトは2度罹りしないこと」を記録しています。このことは非常に重要です。メカニズムはどうであれ、「感染症から回復すると免疫ができ、同じ感染症には罹らない」という事実が理解されていたということです。
免疫の特徴は、自己認識(自己と非自己の識別)と記憶の成立です。免疫系には記憶があり、一度かかると、免疫記憶細胞ができます。その後、同じ病原体に暴露されると、速やかに免疫記憶細胞が分裂・増殖し、迅速に免疫応答が誘導され、同じ感染症には二度はかからないという現象があります。これが軽くかかっておけば、本物の病原性の強い病原体に暴露されても、感染症にかからないという予防ワクチンの開発につながりました。
4、ローマ帝国とペスト
アテネの疫病が、確実にペストであるという証拠はありませんでした。一方、現代の医学で言うペストと同じ症状と推定される最初の大流行は、542年~543年にユスティニアヌス1世(在位527-565年)が統治していた東ローマ帝国(ビザンチン帝国)で起こりました。この時のペストは、いまの臨床症状による分類では腺ペストに入ります。また、ユスティニアヌス自身も感染したため「ユスティニアヌスの斑点」と呼ばれています。ペストはエジプトから、パレスチナ、コンスタンチノープルへと広がり、542年には旧西ローマ帝国の領域に侵入しました。547年にはブリテン島周辺に広がり、フランスへは567年に侵入しています。その後、中近東、アジア等にも広がり、最初の発生から約60年にわたり流行しました。コンスタンチノープルでは、最盛期、毎日5,000~10,000人もの死者が出たといわれています。ユスティニアヌスは回復しましたが、ガリア(フランス)やイギリスへの侵略計画を断念せざるを得ず、「東ローマ帝国により統一ローマを再建しよう」というユスティニアヌス1世の理想は挫折せざるを得ませんでした。
中世のペストをみてみましょう。モンゴル帝国の支配下でユーラシア大陸の東西を結ぶ交易が盛んになったことが、このペスト大流行の背景にあると考えられています。1347年10月、中央アジアからイタリアのシチリア島メッシーナに上陸したペストの流行が最初です。これは、ヨーロッパに運ばれた毛皮についていた蚤が媒介したと考えられています。1348年、アルプス以北のヨーロッパに伝播し、14世紀末まで3回の大流行と多くの小流行を繰り返し、猛威を振るいました。全世界でおよそ8,500万人、当時の欧州の人口の1/3 ~2/3、約2,000万~3,000万人が死亡したと推定されています。人口の激減によりヨーロッパ社会では農奴が不足し、荘園制度が大きな影響をうけました。ペストはイスラム世界にも広がり、当時エジプトを支配していたマムルーク朝(1250~1517年)では、ペストの流行が国家の衰退の一因となりました。
しかし、ペストの流行は、海上検疫という感染症の流行を防止する新しい制度を生み出しました。検疫(quarantine)は、イタリア語のヴェネツィア方言でクアランティーナ(quarantina:約40)およびクアランタ・ジョルニquaranta giorni (40日間)を語源としています。1347年以後のペストの大流行時、ヴェネツィア共和国当局は、この疫病が東洋から来た船から広がることに気付きました。船内にペストの感染者がいないことを確認するため、潜伏期間に等しい40日間、疑わしい船をヴェネツィアやラグーサ港外に強制的に停泊させる措置をとりました。正式な海上検疫は1377年ヴェネツィアで始まりました。当初30日間だったのですが、不十分であるとして、後に40日に変更されました。また、ペストを耐過し、2度と罹らなかった修道僧等は「神の恩寵を授かった人」として患者の世話をしました。
ペスト菌の発見と学名
19世紀末、中国を起源とするペストが世界中にひろがりました。これは雲南省で1855年に大流行した腺ペストが起源とされています。1894年の香港での大流行を機に世界的に流行がおきました。20世紀初頭、中国の東部沿岸地域や台湾、日本、ハワイ諸島、さらにアメリカ合衆国、東南アジアから南アジアの各地にも広がっていきました。この時、ロバート・コッホ研究所から帰国した北里柴三郎は日本政府により香港に調査派遣され(1894)、腺ペストの病原菌を発見しました。ほぼ同時に、パスツール研究所の細菌学者でもあったアレクサンドル・イェルサンもペスト菌を発見・単離し、ペストと結びつけて発表しました。こうして、ペストの原因がはじめて細菌による感染症であることが確定されました。1910年から翌1911年にかけては、清朝末期の満州で肺ペストが流行しています。
ペスト菌の学名エシニア・ペストの名前は以下のようにして決まりました。ペスト菌は1894年にスイス・フランスの医師で、パスツール研究所の細菌学者、アレクサンドル・イェルサンが香港で発見しました。同時期に、コッホの指導を受けた細菌学者の北里柴三郎がこれとは全く独立にペスト菌を発見しています。しかし、ペストとペスト菌を最初に結び付けて考えたのはイェルサンでした。当初パスツールにちなんでパスツレラ・ペスティスPasteurella pestisと名付けられていたこの菌の学名は、1967年に、イェルサンにちなんだイェルシニア・ペスティスYersinia pestisに改められました。
ペストの流行から学んだもの
ペロポネソス戦争時のアテネの疫病や中世の黒死病の時に記された、「ペストから回復した人はペストに二度かかりしない」という免疫現象の理解は、後の予防ワクチン開発につながる経験であったことは前に述べました。
また、中世の医学はヨーロッパよりも、イスラム文化圏で進んでおり、感染症が伝播することを発見したのは、イスラム圏の医学者でサーマーン朝のイブン・スィーナーといわれています。彼が著した「医学典範(1020年)」には、患者を隔離することにより感染症の拡大を止め得ることが記載されています。イブン・アルハティーブは14世紀のイベリア半島のペスト流行時に、汚染した衣類・食器・イヤリングへの接触が発症の有無を左右していることを発見しました。さらに、イブン・ハーティマ(1369年)はペストを見て、「感染症は微生物が体内に侵入することによって発症する」との仮説を打ち立てています。
しかし、実際に目に見えない微生物が存在することは、「微生物学の父」と称されるオランダの商人で役人のアントニ・ファン・レーウェンフック(1632-1723)が、顕微鏡により、多くの微生物(1674年)や精子(1677年)を発見し、記載した時に始まります。
ロバート・コッホがゼラチン等を用いた固体培地に1種類の微生物だけを純粋に分離する、純粋培養法を確立し、炭疽菌、腸チフス菌、結核菌、コレラ菌などを分離しました。また、有名な病原菌に関するコッホの4原則(1876年)を確立し、感染症の原因が細菌によることを証明しました。そして、1894年のペスト菌の分離により、「恐怖の疫病ペスト」の原因がペスト菌の感染によることが明らかにされました。ペストの有効な治療法にはなりませんでしたが、グラム陽性細菌を殺す抗生物質の発見は、1928年のフレミングによるペニシリンの発見以後になります。その後、様々な作用機序(作用のメカニズム)を持つ抗生物質が見つかり、ペスト菌に有効なストレプトマイシンやテトラサイクリンなどの抗生物質が開発されています。
ペストを運ぶ動物
米国では中西部の乾燥地帯で野生のプレーリードッグと蚤の間でペスト菌が行き来しており、ヒトやペット動物が感染を受ける例が毎年のように報告されています。ペストに関しては1999年、米国疾病予防管理センター(CDC)が、日本に輸入されるプレーリードッグにペスト感染の危険性があることを伝えてきました。この頃、米国・カナダから年間13,000頭以上のプレーリードッグが輸入されていました。専門家委員会で、厚生労働省に対し輸入規制の必要があることが提言されました。この提案は2003年1月の閣議で了承され、同年3月1日からプレーリードッグの輸入禁止措置がとられることとなりました。
プレーリードッグは齧歯類、リス科の動物で、北米中西部を中心に米国からカナダに広く分布しています。北米ではプレーリードッグのほかにジリスのグループ、リスのグループなどがペスト菌の宿主となっています。齧歯類といっても、ペスト菌に対する感受性は大きく違います。グループでペスト菌を維持するキャリアー動物群と、ペスト菌が著しく増殖し致命的感染となるペスト菌の増幅動物群がいます。ハタネズミやシカネズミのように、常にペスト菌を保持しているキャリアー動物は、ペスト菌に対して比較的抵抗性が高く、繁殖力が高いので、蚤が通年をとおして活動し、ペスト菌を次世代の動物に移していくと考えられています。他方、ジリス、ウッドラット、プレーリードッグなどは、非常に感受性が高く、ペスト菌の感染により致命的な敗血症を起こしやすい動物種です。これらの動物では、時々、一部のコロニーが全滅してしまうことがあります。
2003年5月、米国でプレーリードッグからサル痘がヒトに感染し、パニックになりました。これはアフリカから輸入した齧歯類(ガンビアラット)がウイルスに感染しており、プレーリードッグに感染させ、そのプレーリードッグがペットとして販売されたためでした。日本は、幸いなことにすでに輸入禁止にしていました。しかし、その後、問題となったガンビアラットは、日本にも輸入されていたことがわかり、厚生労働省は追跡調査をし、日本にはサル痘の侵入がなかったことを確かめました。
まとめ
ペスト菌は、約4,000種いるといわれる哺乳類の中で、最大種数の2,000種を誇る齧歯類と蚤の間で循環している病原体です。現生人類が約6万年前にアフリカから世界中に広がるずっと前から、それぞれの生活環(病原体と自然宿主と媒介動物の関係)をもっていました。人類が数千年以上悩み続けてきた感染症を引き起こす病原体ですが、人類が存在しなくても、これらの病原体は循環し続けるでしょう。すなわち、野生の動物と病原体の循環の中にヒトが組み込まれ感染症として悩むわけです。動物に由来する感染症(人獣共通感染症)の多くが、これに類似した特性を持っており、コントロールすることが難しい理由がここにあります。
今治キャンパスの獣医学部の学生(2年生秋①学期)に、人獣共通感染症を教えているときにニュースがはいりましたので、講義に以下のスライドを1枚加えました。

 吉川泰弘の
ホームページへようこそ!
吉川泰弘の
ホームページへようこそ!








