Bウイルスの日本での感染事例が報告されました。この機会にもう一度Bウイルスのサル、およびヒトへの感染について考えてみることにしました。Bウイルスに関する情報は、以前からそれほど増えているわけではありませんが、ゲノム情報やαヘルペスウイルスの特性、蛋白機能などの情報は新しいものがありました。2020年1月、Bウイルスの講演をする機会があったので、もう一度スライドを作りなおしました。
Bウイルスの説明に入る前に紹介したいことがあります。これまで動物のヘルペスウイルスで、ヒトに脳炎のような致命的な感染症を起こすのは、マカカ属サル類に由来するBウイルスのみと報告されてきました。しかし、2019年中国から最近、豚のヘルペスウイルス(オーエスキー病ウイルス、仮性or 偽狂犬病ウイルス、豚ヘルペスウイルス1の名前を持つウイルス)がBウイルスと同様、ヒトに急性脳炎を起こすことが報告されました。以下にデータの概要を提示しておきます。













先日、Bウイルス抗体陽性のサル類を実験に使うに当たっての考えかたを聞かれました。 簡単に説明しましたが、かなり前に学会で発表したことを思い出して、このスライドを渡しました。今、見直しても、内容的には、現在でも変わっていないので、ここに掲載します。
Bウイルス抗体陽性のサル類を実験に使う必要のある研究者の役に立てば幸いです。

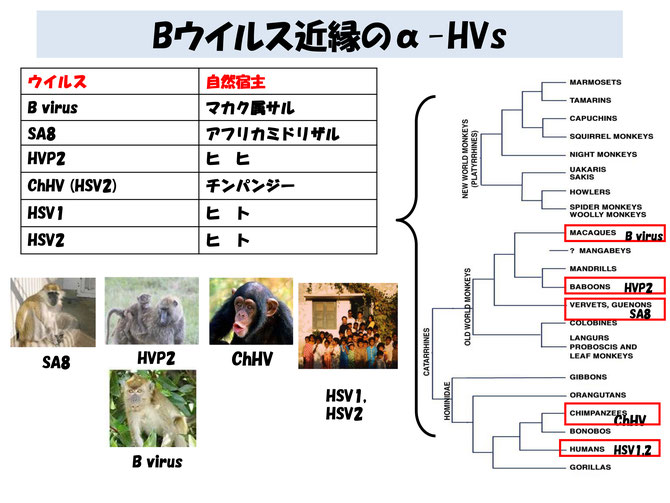
Bウイルスはアジア産マカカ属のサル類のヘルペスウイルスです。人は2種類の単純ヘルペスウイルスを持っています(HSV1, HSV2).HSV1は主に顔面ヘルペスとして口唇や口腔、顔面に病変を出します。HSV2は性器ヘルペスで生殖器に病変を出します。
ヘルペスウイルスは軟体動物の牡蠣から魚類(鯉ヘルペス)、鳥類、哺乳類まで多くの動物がウイルスを保有しています。宿主特異性が強く、動物種を超えて感染することは少ないですが、時に種を超えると中枢神経系を巻き込み重症化します。また、自然宿主では感染後、神経節に潜伏感染し、ストレスや免疫低下に伴い再活性化します。
人に近年な、チンパンジーはChHVを持っていますが、表面蛋白は人のHSV2に近いといわれています。ヒヒはHVP2ウイルス、アフリカミドリザルはSA8,マカカ(マカク)属のサルはBウイルスを保有しています。
Bウイルスが属するヘルペスウイルスは、2重鎖のDNAウイルスで、通常のウイルス(最近見つかった、小型細菌よりも大きなメガウイルスを除いて)では、ポックスウイルスについで大きなウイルスです。ゲノムサイズはポックスウイルスの約半分ですが、コードしている遺伝子は80種類以上(ポックスウイルスは約200種類、通常のウイルスは10種類くらい)という複雑なウイルスです。
図にあるように、エンベロープには多種類の糖蛋白質、内側にテグメント蛋白、さらに内側に通常のウイルスのようなカプシド構造があり、カプシド内にウイルスDNAがあります。
皮膚や粘膜から感染したウイルスはエンベロープを細胞膜と融合させ細胞に侵入します。膜融合により感染した細胞内にはテグメント (tegument)とヌクレオカプシ(nucleocapsid)が放出されます。ウイルスゲノムは核内に入り、核内でDNA複製、mRNAへの転写、ウイルス蛋白合成が進み、次世代ウイルスが作られます。

ヘルペスウイルスのエンベロープ(外殻)に埋まっている蛋白質には10種類以上の糖蛋白質(スパイク)があります。通常のウイルスの糖蛋白質は1種類か2種類くらいです(例えばインフルエンザウイルスのHA, 麻疹ウイルスのHA, F, SARSウイルスのSなど)。糖蛋白質のうちgB,gD,gHは細胞表面の受容体蛋白質と結合し、ウイルスが細胞に侵入する際に使われます。gEは抗体の定常部分にあるFc領域に対する受容体活性があります。gCは特異的なウイルス受容体というより、一般的な組織構造分子であるへパラン硫酸を介した細胞への吸着作用や、活性化した補体の主要成分であるC3bに対する受容体活性を示します。
通常のウイルスでヘルペスウイルスのテグメントに相当するのは、マトリックス(M)蛋白です。ウイルス粒子のエンベロープとカプシド(あるいはヌクレオカプシド)の間を埋めています。ヘルペスウイルスのテグメントには20種類以上の構造蛋白が含まれます。主な役割は細胞の転写因子に作用してウイルスの前初期遺伝子群の発現増強や、細胞のmRNAから蛋白への合成(翻訳)を阻害し、ウイルスのmRNAを翻訳させる(vhs:virual
host shutoff)働きをします。
カプシド(ウイルスのカプセル構造)蛋白は正二十面体構造を形成し、その主要蛋白はVP5ですが、 5種類の蛋白(VP5、VP23、VP19C、VP26、VP24)から出来ています。
一番内側は、コア(芯)となる部分で、足場蛋白(scaffoldings)となるVP21やVP22a TK(チミジンキナーゼ、核酸のチミジンをリン酸化する) 、ヘリカーゼ (2重螺旋を作る)、DNAポリメラーゼ(DNA合成酵素)などと、ヘルペスウイルスのゲノムDNAが入っています。






















Bウイルス感染症 (ヘルペスウイルスB感染症)
1 病名:Bウイルス感染症(B virus disease)。
2 定義:Bウイルス(BV)はherpesvirus simiaeとも言われる。アジアに生息するマカカ属サル類が保有するαヘルペスウイルスであり、ヒトの単純ヘルペスウイルス(HSV-1, HSV-2)や、ヒヒヘルペスウイルス(HVP)、アフリカミドリザルヘルペスウイルス(SA8)と近縁のウイルスである。しかし、BVは中枢神経を冒す重要な人獣共通感染症であり、本ウイルスを排出しているサルから咬傷・体液の飛沫などでヒトが感染し神経症状を呈すると、死亡率は70%と非常に高い。最近、抗ヘルペス薬のアシクロビル、ガンシクロビル、バラシクロビルなどが治療に有効であることが明らかにされ、以前ほどの死亡率ではなくなった。
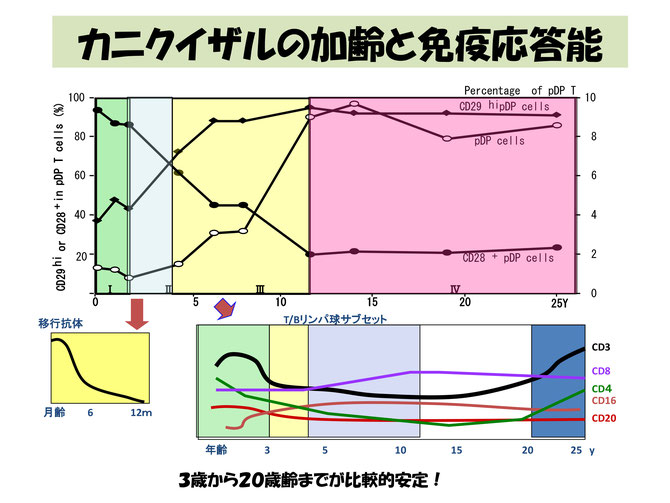
3 概要:BVはアカゲザル、カニクイザルで多く分離される。ニホンザル、タイワンザル、ブタオザル、ベニガオザル、ボンネットザルからも分離されている。疫学的には未成熟サルでBVに感染している例は少ない。移行抗体のある幼若期に母親から分離する(母子分離)とBVフリーのサルを飼育することが出来る。しかし、群飼育の場合は性成熟に達するまでにウイルスは母親から伝播し、若齢個体間で水平感染し、成体では80~90%が抗体陽性となる。他方、動物園のサル山で飼育されているニホンザルでは、ウイルスフリーの群れや、次世代にウイルスが拡がらないケースもみられる。感染したBVは三叉神経節等に潜伏する。本藤らが厚生省の研究班で抗体陽性カニクイザル(30例)の三叉神経節についてウイルスゲノムの検出を試みたところ、約半数以上の個体でウイルスゲノムの存在が証明された。しかし、ウイルス蛋白発現を伴う活性化状態のものは見られなかった1)。一般に感染したサルは神経節等に一生ウイルスを保有すると考えられている。
ヒトのBV感染症は1932年、米国で1研究者が、アカゲザルに咬まれ急性進行性髄膜脳炎で死亡したケースが最初である。BVは、その研究者の名前(William Brebner)の頭文字をとって命名された2)。その後、30~40例(いずれも米国)が報告されている。1973年までの症例は17例で、12例は50年代後半に起こっている。これは、ポリオウイルスワクチンの製造・検定が始まり、アカゲサルなど多くのアジア産の野生捕獲サル類が使用されるようになった時期である。
やがて、バイオハザードの概念がひろがり、麻酔薬、挟体板ケージ、防護衣や手袋の着用が普及するにつれ、1973年~1987年にかけて感染例はわずか数例に減少した。その後AIDS(acquired immunodeficiency syndrome: 後天性免疫不全症候群)動物モデルなどの研究が盛んになり、サル類使用数の増加、BVに十分な知識を持たない研究者や飼育者が実験に加わった結果、BV感染例が増加した。1987年にフロリダ州で4人、1989年にミシガン州で3人の集団感染が起こった。その後1991年、1997年に各1人の感染死亡例が報告されている。
4 病因:BVはアルファヘルペスウイルス亜科(Alphaherpesvirinae)に属する二本鎖DNAウイルスで、エンベロープを持ちウイルス粒子の大きさは120〜200nm、カプシドは100〜110nmの正20面体構造である。ヒトの1型単純ヘルペスウイルス(HSV-1)に高い共通抗原性を有し、発育鶏卵の漿尿膜にポックを形成する。培養細胞(ウサギ腎、サル腎、HeLa細胞など)では円形化と細胞の脱落、融合巨細胞形成が見られる。多核巨細胞の核内にはしばしば好酸性封入体が出現する。BVはホルマリンで容易に不活化(4,000倍に希釈したホルマリンで36℃、48時間で完全に不活化)される。実験感染では新世界ザル、アフリカ産サル類が致死的経過をとる。ウサギは非常に感受性が高く、どのような経路で接種しても5~12日後に致死的麻痺を起こす。新生仔マウスも高い感受性を示す。自然宿主であるアジア産のマカカ属サル類では持続感染(潜伏感染)し、ウイルスは終生にわたって神経節に残存する。宿主の免疫機能が低下した際や過度のストレスがかかると再活性化する。
5 動物の感染症:アジア産マカカ属サル類のBV初感染では、最初に舌の背側、口唇の粘膜・上皮移行部、口腔粘膜、時には皮膚に小さな水疱を生じる(図1)。この病巣は直ちに潰瘍となり、痂皮が形成され7〜14日で治癒する。通常は不顕性感染が多い。重篤な場合は神経症状を呈することがある。他方、新世界ザル、アフリカのサル類、類人猿はBVに感染すると、ヒトと同様に神経症状を呈し死亡する。
病理学的には感染局所の上皮細胞に空胞変性、壊死、核内封入体がみられる。多核巨細胞もしばしば認められる。全身感染において内臓では、肝に壊死巣と核内封入体がみられる。中枢神経系では、三叉神経の下行路と神経核に壊死、囲管性細胞浸潤、グリオーシスがみられる。また、封入体がグリア細胞、神経細胞の核内に認められることがある。
口唇、舌、口腔粘膜の特徴ある病巣により、ある程度診断がつく。病理組織学的変化も診断に有効である。病変部、口腔拭い液、膣拭い液などからのウイルス分離により確定診断がされる。BVは感染サルの結膜、頬粘膜、生殖器などから、それぞれ同じくらいの頻度で分離される。BV抗体陽性個体の飼育およびサル類からの検査材料の採取はBSL(biosafety level)のレベル2で、生きたウイルスの分離・診断はレベル3で行われるが、ウイルスの増殖・大量培養にはP4(physical containment 4)の研究施設が必要である。血清診断としては抗体の検出がある。ウイルス中和試験はリスクが高く、現在わが国では行われていない。従来HSV-1を抗原とした補体結合試験が行われてきたが、現在は米国から輸入した不活化BV抗原を用いたELISA法が、高感度で再現性が優れているために多用されている。BVと交差反応性の高いアフリカミドリザルのヘルペスウイルスやヒヒのヘルペスウイルスが不活化BV抗原の代わりに利用されることもある。予防、治療は行わない。
6 ヒトの感染症:ヒトのBV感染は、これまで70%以上の致命率であったが、感染初期の抗ウイルス薬(アシクロビル、ガンシクロビル、バラシクロビル)による治療や維持療法の進歩で致命率は低下している。典型的臨床経過は、前駆症状として暴露後1~2日目に傷口に水疱が出現し、潰瘍形成、局所リンパ節の腫脹をみることがある。その後、平均10~20日の潜伏期で発熱、頭痛、悪感などの症状と共に筋肉痛、めまい、燕下困難、腹痛などの神経症状を示す。その後、下半身麻痺から上向性に麻痺が進行し肺虚脱で死亡する。通常、発症後2~30日で死亡する。感染耐過したヒトでは重度神経後遺症がみられる。病理組織学的には脳と脊髄の広範な変性と壊死、時に核内封入体が見られる。病変だけでは、ヒトの単純ヘルペス脳炎との鑑別は困難である。肝、脾、リンパ節、副腎に巣状壊死が出現することがある。時にこれら病変部に核内封入体が出現する。
ヒトへの感染が疑われる例ではBVとHSV-1,2が交差反応するため、BVの感染を血清学的に診断することが困難である。ヒト血清をHSV-1で吸収することにより交差反応性を低下させ、ELISAやウエスタンブロット法でBV特異抗体やBV特異的蛋白バンドを検出する方法も試みられているが、神経症状の出現とウイルス分離なしで確定診断するには不十分である。最近は、PCR法と制限酵素を用いたRFLP(restriction fragment length polymorphism: 制限酵素切断による断片長多型)により、HSVとBVを鑑別診断する試みがなされている。本藤らは糖蛋白をコードする遺伝子領域を対象にPCR-ハイブリダイゼーション法により非常に高感度で特異性の高い鑑別法を開発している3)。また、PCR法は糖蛋白領域遺伝子を対象にした場合、病変部のウイルスゲノムの存在とBVの鑑別に有効であること、ウイルス分離が陰性の場合でもBV感染の早期診断に実用的であることが報告されている。
1977年に、全身投与可能なアシクロビルが発売された。アシクロビルはウイルスのチミジンキナーゼによりリン酸化され、ウイルスのDNAポリメラーゼを特異的に阻害する。ヒトがBVに感染した場合は、ヘルペスの治療に使用されるアシクロビル、ガンシクロビルが有効である。1987年〜1994年の間に臨床検査で感染が確認された5人のBV感染者は、中枢神経系の症状の初期段階あるいは発生後に、高用量のアシクロビルまたはガンシクロビルの静脈内投与を受けた。この5人に見られた症状は、治療開始後2~3週間で消失した。1987年の二次感染例では、皮膚科の診断後、直ちにアシクロビルの経口投与を始め、BVの感染が確定してからは、アシクロビルの静脈注射が行われ回復した。また最近、アシクロビルの代わりに経口投与で吸収効率のよいバラシクロビルの使用が推奨されている。
7 公衆衛生と法規:BVに暴露されたと思われ、臨床症状がない場合、および症状が出ている場合に、抗ウイルス剤をどのような用量でどう投与すべきかについては、米国からBV感染による発病の予防法と治療法に関するガイドラインが出ており、日本語に訳されている4)。
BV感染症は感染症法で四類感染症に分類されており、BVに感染した患者を診断した医師は7日以内に保健所に届け出る義務がある。また検疫中にBV病を発症したサル類を発見した獣医師は届け出るよう通達が出されている。さらに、病原体取扱い基準ではBVは三種病原体に分類されているので、所持などの届け出が必要である。
8 事故時の対応と予防:アジア産のサル類に咬まれた場合は、局所の洗浄、消毒などの応急処置をとった後、原因となったサル類がBV抗体を保有しているか否か(一社)予防衛生協会に検査を依頼する。病院に行き、採血し血清を保存する。当該サルがBV抗体陽性であり、その後、数日して創傷部の水疱や違和感、痺れなどの症状が出るようであれば、医師は医薬基盤研の筑波霊長類センターに連絡し、この時点でもう一度採血する。保存血清と新たに得た血清および水疱など病巣の拭い液(綿棒で吸い取り、チューブに保存)を2重のチューブにいれ、スチロール箱を使用してクール宅急便で霊長類センターに送る。
BV抗体陽性のマカカ属サル類を取り扱うには、挟体板付きケージを使用し、麻酔下で手袋、マスク、ゴーグル、ビニール前掛けなどを使用し慎重に取り扱う必要がある。免疫抑制剤の投与によってBVが再活性化され、本病が誘発されたというカニクイザルの報告があること、ボンネットモンキーのD型レトロウイルス流行による免疫抑制でBV感染の集団発生が起こったことから、BV抗体陽性の個体を免疫抑制などの実験に使用することは避け、BVフリーのSPF動物(specific pathogen free動物:特定病原体フリー動物)を使うべきである。
(吉川泰弘)
文献
1) Prevalence of herpes B virus genome in the trigeminal ganglia of seropositive cynomolgus macaques. Laboratory animals. 42, 99-103 2008
2)Jason D. Pimentel, Herpes B virus — “B” is for Brebner: Dr. William Bartlet Brebner (1903–1932). Canadian Medical Association Journal. 178, 734 2008
3)Oya, C., Ochiai, Y., Taniuchi, Y., Tanaka, T., Ueda, F., Yoshikawa, Y., Hondo, R. Specific detection and identification of herpes B virus by a PCR-microplate hybridization assay.
J. Clin. Microbiol. 42, 1869-1874, 2004
4)長 文昭訳:Bウイルスに接触し感染するかもしれない人のための予防法と治療法
のガイドライン、オベリスク増刊号、1997
 吉川泰弘の
ホームページへようこそ!
吉川泰弘の
ホームページへようこそ!








